Responsable de Laboratorio Ingeniería de Tejidos y Biología Sintética
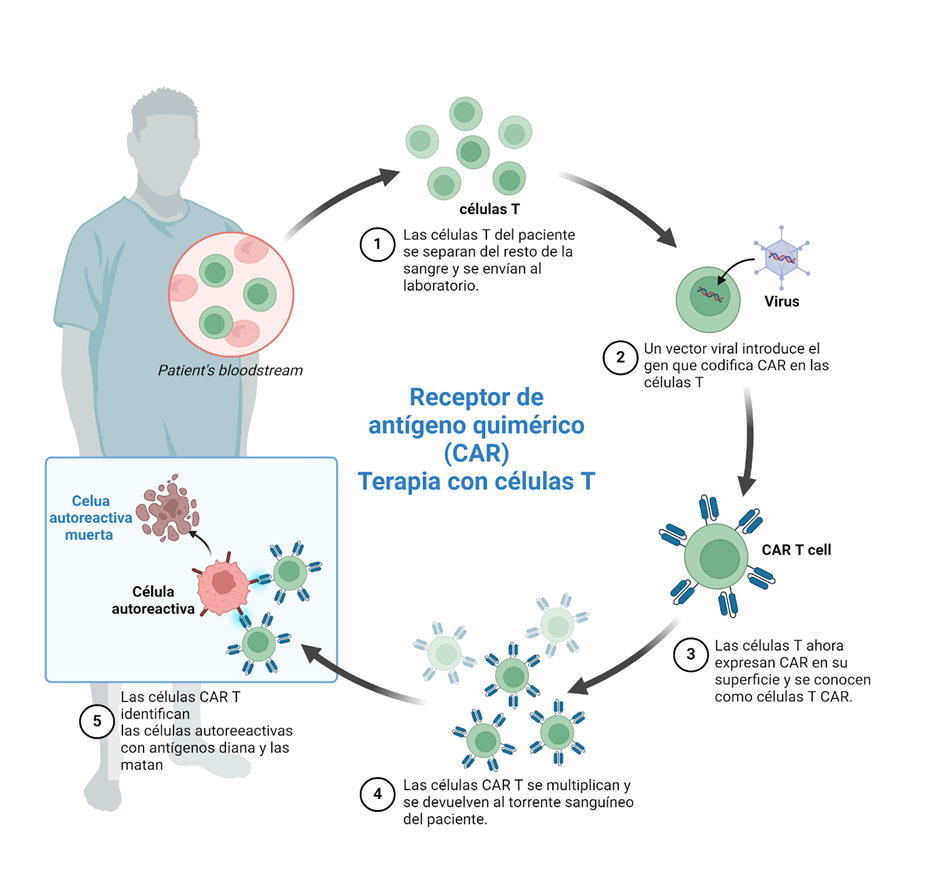
Los Receptores de Antígenos Quiméricos (CAR por sus siglas en inglés) son receptores diseñados mediante técnicas de ingeniería genética, con el objetivo de dirigir principalmente, linfocitos T y células NK, para que reconozcan y eliminen células que expresan un antígeno específico. La unión del CAR a los antígenos objetivo presentes en la superficie celular ocurre independientemente del complejo mayor de histocompatibilidad (MHC), lo que resulta en una activación robusta de las células T y en respuestas inmunes poderosas.
Los cuatro componentes principales de los receptores CAR son:
- Dominio de unión al antígeno diana extracelular: Le confiere la especificidad para unirse a un antígeno determinado. Para reconocer un antígeno determinado e inducir la activación de las células T, la afinidad de unión al antígeno de los CAR debe ser lo suficientemente alta, pero no lo suficientemente alta como para provocar la muerte inducida por la activación de las células T que expresan CAR y desencadenar toxicidades.
- Región bisagra: Brinda flexibilidad y contribuye a la longitud para permitir que el dominio de unión al antígeno acceda al epítopo objetivo.
- Dominio transmembrana: Su función más estudiada es anclar el receptor CAR a la membrana del linfocito T.
- Uno o más dominios de señalización intracelular: Los dominios coestimuladores más comunes son CD28 y 4-1BB (CD137); los cuales están asociados con altas tasas de respuesta del paciente.
El proceso de manufactura de las células CAR-T, inicia con el aislamiento de las células mononucleares periféricas (PBMCs), mediante la técnica de gradiente de densidad Ficoll- Paque o por leucoféresis, luego los linfocitos T CD4+ y/o CD8+ dependiendo del producto deseado, se hace un enriquecimiento y activación, para lo cual se expone a las células a anticuerpos activadores de anti-CD3 y anti-CD28 unidos a perlas. Para luego realizar las modificaciones genéticas de las células T aisladas, mediante enfoques virales o no virales.
Los trastornos autoinmunes son una categoría amplia de enfermedades con patología compleja. Estos trastornos se desarrollan cuando las propias células inmunitarias del cuerpo (en particular, las células B y T autorreactivas) inician ataques anormales en sus propios tejidos a través de una variedad de vías efectoras. Estas enfermedades surgen de una combinación de predisposición genética y factores ambientales.
Para evitar que las células inmunes autorreactivas ataquen los órganos del huésped, el tratamiento de las enfermedades autoinmunes sigue siendo utilizar medicamentos inmunosupresores amplios, generalmente no dirigidos, como glucocorticoides y medicamentos antiinflamatorios no esteroides, o su bloqueo con anticuerpos específicos, como por ejemplo anticuerpos contra CD20 (Rituximab) o BAFF (Belimumab), anticuerpos contra células T, como anti CD52 (alemtuzumab), o contra citoquinas proinflamatorias como anticuerpos contra TNF- a (infliximab). También se puede tratar las enfermedades autoinmunes, mediante trasplante de células hematopoyéticas que puede ser autólogo o alogénico.
La terapia celular para enfermedades autoinmunes tiene dos enfoques; eliminar y amortiguar a las células inmunes autoreactivas.
En un reciente artículo publicado en The New England Journal of Medicine, investigadores trataron a 8 pacientes con Lupus eritematoso sistémico, 3 pacientes con miositis inflamatoria idiopática y 4 pacientes con esclerosis sistémica; con una dosis única de infusión de células T del receptor quimérico (CAR) CD19. Todos los pacientes del estudio habían tenido respuesta negativa a al menos dos tratamientos inmunosupresores previos.
Nueve días después de la infusión las células CAR T alcanzaron picos de concentraciones (146 por microlitro), siendo las células B CD19+ eliminadas de la sangre periférica después de 7 días.
Después de seis meses los pacientes con Lupus eritematoso sistémico, presentaron remisión, estando ausente la enfermedad por 29 meses. En los tres pacientes con miositis inflamatoria idiopática después de tres meses los niveles de creatinin kinasa y la función muscular se normalizaron, todos los pacientes descontinuaron corticoides y otros medicamentos inmunosupresores.
Los datos mostrados en este estudio proveen nueva evidencia de la seguridad y eficacia a corto término de la terapia con células CAR-T cell CD19 para enfermedades autoinmunes, pero estudios clínicos son necesarios.
Bibliografía
- Blache, U. et al. (2023) ‘CAR T cells for treating autoimmune diseases’, RMD Open, 9(4), pp. 1–9. Available at: https://doi.org/10.1136/rmdopen-2022-002907.
- De Marco, R.C., Monzo, H.J. and Ojala, P.M. (2023) ‘CAR T Cell Therapy: A Versatile Living Drug’, International Journal of Molecular Sciences, 24(7), pp. 1–22. Available at: https://doi.org/10.3390/ijms24076300.
- Müller, F. et al. (2024) ‘CD19 CAR T-Cell Therapy in Autoimmune Disease — A Case Series with Follow-up’, The New England Journal of Medicine, 390(8), pp. 687–700. Available at: https://doi.org/10.1056/NEJMoa2308917.